- Los betabloqueantes son antagonistas competitivos de los receptores beta-
adrenérgicos; no obstante, no se comportan como un grupo único de fármacos y se
reconocen diferencias relevantes entre las distintas moléculas.1 - Estas diferencias se relacionan con sus efectos específicos sobre los receptores beta-
adrenérgicos y por la existencia de mecanismos complementarios de acción. 1
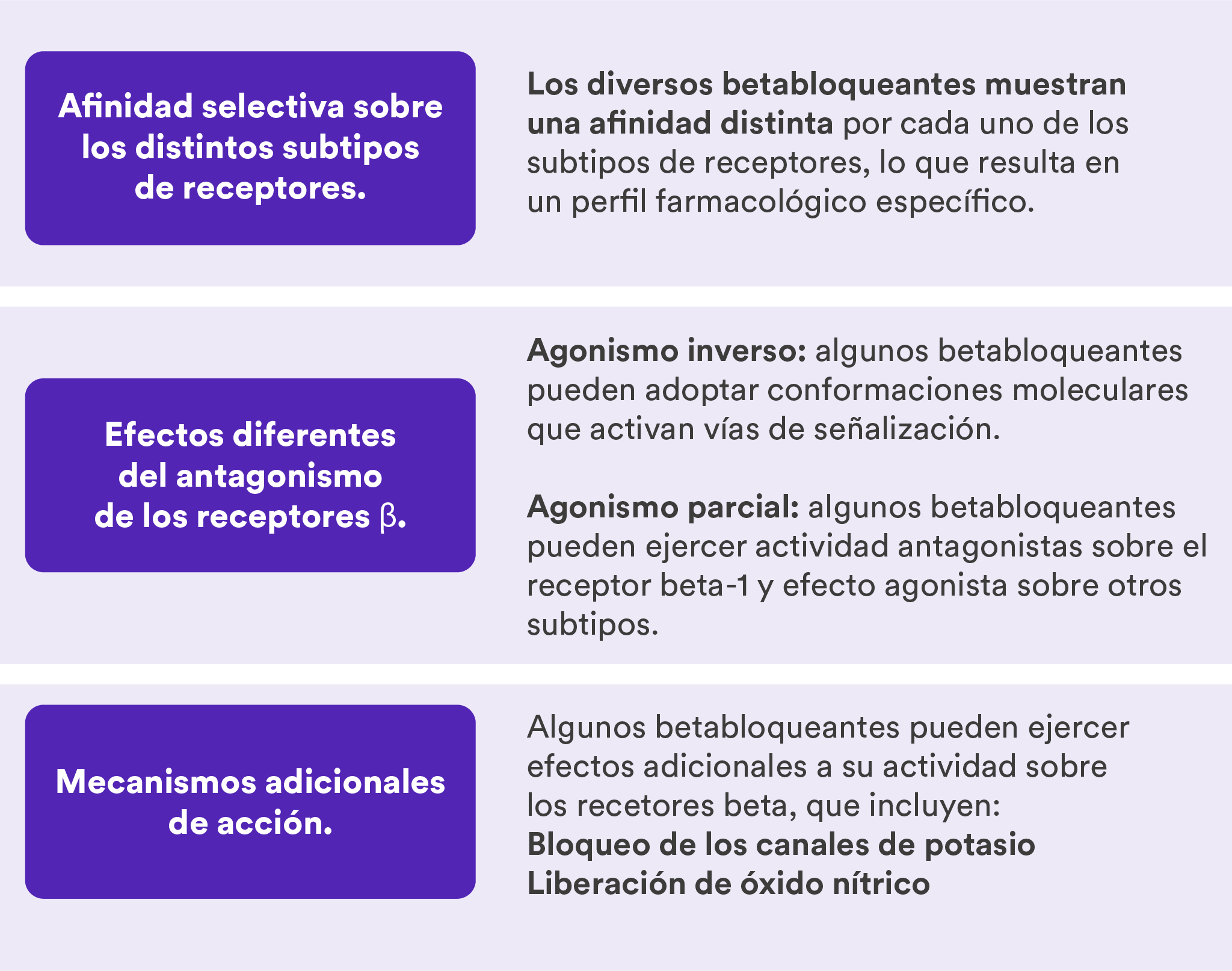
- Como consecuencia y en función fundamentalmente de las diferencias de actividad
sobre los subtipos de receptores β1 y β2, los betabloqueantes pueden clasificarse en:
|
Actividad vasodilatadora |
Fármaco |
Mecanismos complementarios |
|
|
β1 y β2 selectivos |
Ausente |
Alprenolol |
|
|
Bupranolol |
|||
|
Nadolol |
|||
|
Orprendol |
|||
|
Pindolol |
|||
|
Propranolol |
|||
|
Sotalol |
Acción sobre los canales de potasio |
||
|
Timolol |
|||
|
Presente |
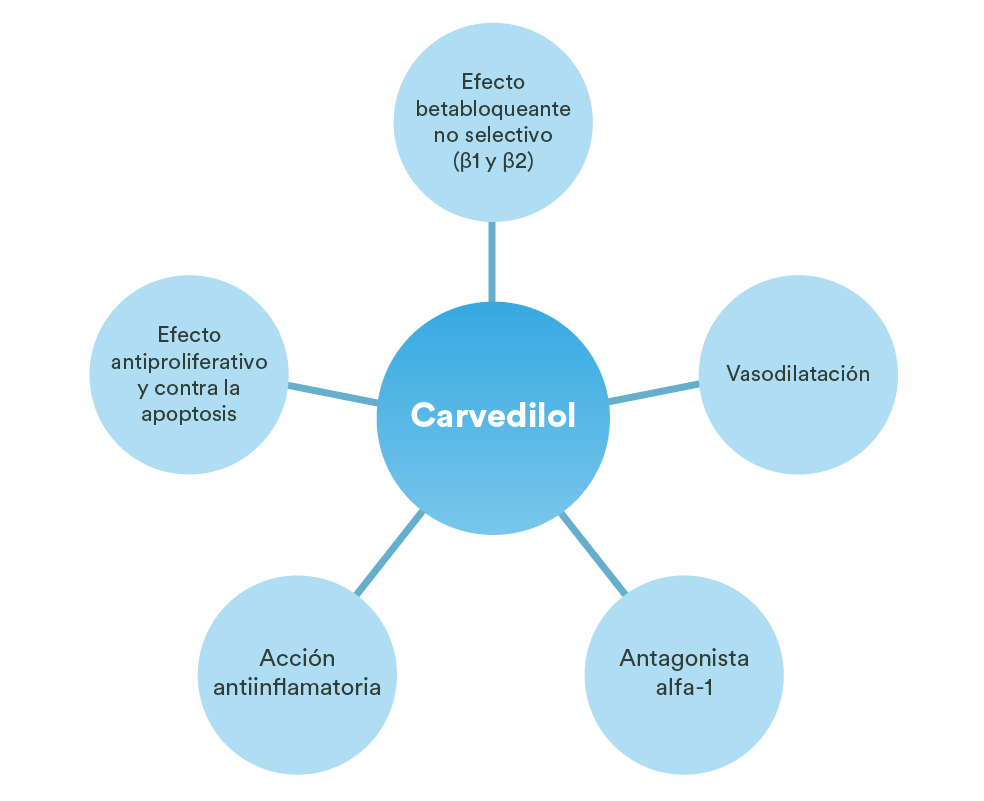
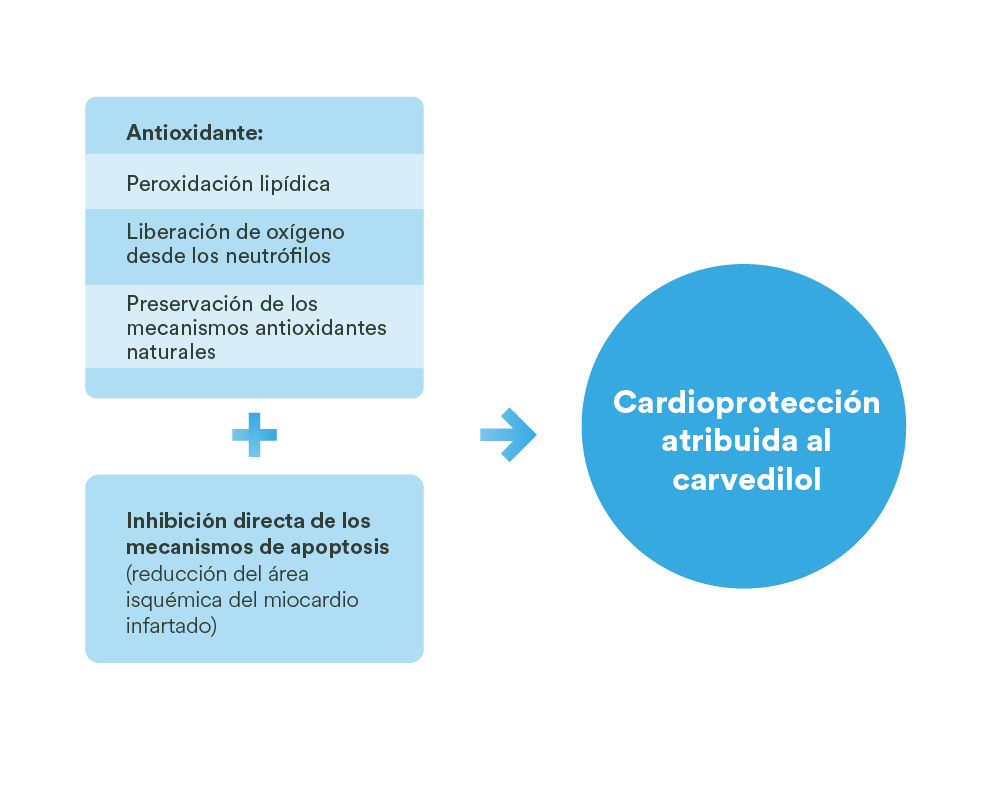
Carvedilol |
Antagonista alfa-1, liberación de óxido nítrico |
|
|
Labetalol |
Antagonista alfa-1 |
||
|
β1 selectivos |
Ausente |
Atenolol |
|
|
Betaxolol |
|||
|
Bisoprolol |
|||
|
Metoprolol |
Efectos sobre el receptor alfa-2 |
||
|
Presente |
Nebivolol |
Estas características permiten reconocer indicaciones cardiovasculares diferenciadas para cada uno de los betabloqueantes:
|
β1 y β2 selectivos |
β1 selectivos |
|||
|
Sin actividad vasodilatadora |
Con actividad vasodilatadora |
Sin actividad vasodilatadora |
Con actividad vasodilatadora |
|
|
Insuficiencia cardíaca |
Carvedilol |
Bisoprolol Metoprolol |
Nebivolol |
|
|
Hipertensión |
Propranolol Nadolol |
Carvedilol Labetalol |
Atenolol Bisoprolol Metoprolol |
Nebivolol |
|
Hipertensión ocular |
Timolol |
Betxolol |
||
|
Cardiopatía isquémica |
Propranolol Nadolol |
Carvedilol |
Atenolol Bisoprolol Metoprolol |
Celiprolol |
|
Arritmias |
Propranolol Nadolol Sotalol |
Atenolol Metoprolol |
||
En el caso de la insuficiencia cardíaca, se considera a los betabloqueantes un pilar fundamental del tratamiento en los estadios avanzados, en forma independiente de la capacidad funcional. Se priorizan aquellos con eficacia demostrado en estudios clínicos, como el carvedilol.
En los pacientes con hipertensión arterial (HTA), los betabloqueantes se reconocen como indicación recomendada en situaciones específicas:3
- HTA asociada a enfermedad coronaria (clase I, nivel de evidencia A)
- HTA asociada a insuficiencia cardíaca o disfunción sistólica ventricular izquierda (clase I, nivel de evidencia A)
- HTA asociada a fibrilación auricular (clase I, nivel de evidencia A)
- HTA en pacientes con migraña (propanolol, clase I, nivel de evidencia C)
- HTA gestacional (labetalol, clase I, nivel de evidencia B)
- HTA y crisis hipertiroidea (clase I, nivel de evidencia C)
- HTA asociada a hiperactividad simpática (clase IIa, nivel de evidencia C)
|
Los betabloqueantes constituyen uno de los grupos de fármacos más útiles en la práctica clínica; a medida que se conocen sus mecanismos de acción intracelulares específicos, mayor es el número de sus potenciales aplicaciones en el tratamiento. Estos fármacos deben entenderse como moléculas individuales y no como un grupo homogéneo de moléculas con una acción terapéutica común.1 |
Referencias:
[1] Oliver E, Mayor Jr F, D’Ocon P. Bloqueadores beta: perspectiva histórica y mecanismos de acción. Rev Esp Cardiol. 2019; 72(10): 853–62.
[2] Sociedad Chilena de Cardiología y Cirugía Cardiovascular y Ministerio de Salud. Guía Clínica: Insuficiencia Cardíaca, 2015.
[3] Sociedad Argentina de Cardiología. Federación Argentina de Cardiología. Sociedad Argentina de Hipertensión Arterial. Consenso Argentino de Hipertensión Arterial. Rev Arg Cardiol. 2018; 86(Supp 2): 1-56.
R1284222-CH-CO-20082024-0850
Material para uso exclusivo de los profesionales de la salud.